EU odobrila kombinirano cepivo mRNA proti gripi in covidu
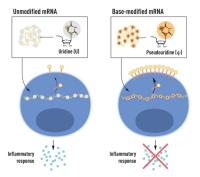
Slo-Tech - Evropska agencija za zdravila je minuli teden odobrila prvo kombinirano cepivo mRNA proti gripi in covidu. Cepivo mCOMBRIAX je razvila Moderna in bo odslej na voljo v vseh državah Evropske unije, na Islandiji, v Liechtensteinu in na Norveškem. Pristojni odbor je že februarja izdal pozitivno mnenje, zato je bila končna odobritev bolj ali manj le vprašanje časa.
Zeleno luč so prižgali po rezultatih tretje faze kliničnih testov, v katerih je sodelovalo 4000 ljudi. V kontrolni skupini so ljudje, stari med 50 in 64, prejeli standardno cepivo proti gripi, medtem ko so starejši od 65 let dobili povišane odmerke standardnega cepiva proti gripi. V obeh skupinah je mCOBRIAX vzpodbudil statistično značilno močnejši imunski odziv.
V ZDA cepivo še lep čas ne bo dostopno. Moderna je sicer vložila prijavo na FDA, a so nato maja lani prijavo umaknili, ko je FDA zahtevala dodatne podatke. Doslej prijave še niso ponovno vložili, k čemur je prispeval tudi negativni odnos oblasti do cepiv, ki ga...
Zeleno luč so prižgali po rezultatih tretje faze kliničnih testov, v katerih je sodelovalo 4000 ljudi. V kontrolni skupini so ljudje, stari med 50 in 64, prejeli standardno cepivo proti gripi, medtem ko so starejši od 65 let dobili povišane odmerke standardnega cepiva proti gripi. V obeh skupinah je mCOBRIAX vzpodbudil statistično značilno močnejši imunski odziv.
V ZDA cepivo še lep čas ne bo dostopno. Moderna je sicer vložila prijavo na FDA, a so nato maja lani prijavo umaknili, ko je FDA zahtevala dodatne podatke. Doslej prijave še niso ponovno vložili, k čemur je prispeval tudi negativni odnos oblasti do cepiv, ki ga...