Prihodnji mesec v ZDA redna odobritev prvega cepiva proti covidu-19
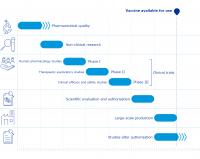
Slo-Tech - Vse registrirana cepiva proti covidu v Evropi in ZDA imajo trenutno izredno odobritev (emergency use authorization) oziroma pogojno odobritev (conditional authorization), ki se uporabi, kot za hudo bolezen ali javnozdravstveno krizo ni drugega odobrenega medicinskega izdelka. Tovrstna odobritev se uporabi, ko pričakovane koristi od uporabe zdravila ali cepiva pretehtajo morebitna tveganja, ki jih lahko povzroči uporaba. Cepiva proti covidu so bila odobrena na tak način, da so lahko hitreje prispela na trg, sicer bi nanje čakali vsaj do prihodnjega meseca.
Ameriška Agencija za hrano in zdravila (FDA), ki nastopa kot regulator, bo septembra cepivu podjetij Pfizer/BioNTech bržkone izdala običajno odobritev. S tem bo to prvo cepivo, ki bo tudi redno registrirano za boj proti covidu-19. Po neuradnih podatkih se bo to zgodilo do 6. septembra, ko v ZDA praznujejo praznik dela. Za samo uporabo cepiva takšna odobritev ne bo prinesla večjih sprememb, bo pa družbenih učinkov kar nekaj....
Ameriška Agencija za hrano in zdravila (FDA), ki nastopa kot regulator, bo septembra cepivu podjetij Pfizer/BioNTech bržkone izdala običajno odobritev. S tem bo to prvo cepivo, ki bo tudi redno registrirano za boj proti covidu-19. Po neuradnih podatkih se bo to zgodilo do 6. septembra, ko v ZDA praznujejo praznik dela. Za samo uporabo cepiva takšna odobritev ne bo prinesla večjih sprememb, bo pa družbenih učinkov kar nekaj....